【研究】在實驗室中首次培育的蝙蝠類器官——探索蝙蝠為什么能夠與病毒一起生活而自身卻不生病?
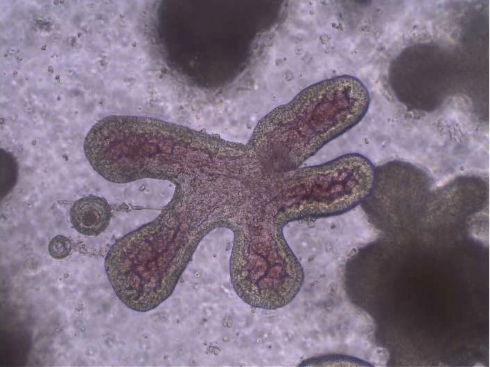

導讀:各種病原體,如埃博拉病毒,馬爾堡病毒,尼帕病毒,亨德拉病毒,嚴重急性呼吸綜合征冠狀病毒(SARS-CoV),中東呼吸綜合征冠狀病毒(MERS-CoV)和SARS-CoV-2,都在威脅人類全球健康。這些病原體的天然宿主被認為是蝙蝠。現在,研究人員從一種果蝠——棕果蝠腸道細胞中培育出類器官。已建立的類器官成功地概括了腸上皮結構和形態的特征,并確定了長期穩定培養所必需的適當補充劑。在實驗接種中,類器官顯示出對PRV的易感性,但對SARS-CoV-2不敏感。這是建立果蝠腸類器官的可擴展類器官培養系統及其對蝙蝠相關病毒,PRV和SARS-CoV-2的敏感性的第一份報告。該類器官是闡明新興的果蝠相關病毒如埃博拉病毒和馬爾堡病毒的耐受機制的有用工具。
試圖解釋為什么蝙蝠一次可以感染許多病毒而不會死于COVID-19等疾病的實驗——這些知識可以幫助我們減少傳染病對人類的威脅——直到現在,人們一直在努力,因為活的野生蝙蝠不是很好的研究對象。為了克服這一障礙,研究人員首次培育出了果蝠屬蝙蝠的“類器官”,它可以在體外繁殖腸道。
一篇描述蝙蝠類器官生長技術的論文發表在《International Journal of Molecular Sciences》上。

https://www.mdpi.com/1422-0067/22/19/10763
蝙蝠是大量人類病原體的天然來源(或者,用流行病學術語來說,“宿主”——病原體在其中存活而不引起疾病的宿主)。這些病毒包括導致許多疾病的病毒,如埃博拉病毒,馬爾堡病毒,尼帕病毒,亨德拉病毒,SARS病毒,MERS病毒和新型冠狀病毒肺炎病毒。事實上,一只蝙蝠可以攜帶這些病毒而不生病。為什么蝙蝠能夠與這么多病毒一起生活而自身卻不生病,仍然是病毒學及其鄰近學科的一大謎團之一。使用單個蝙蝠詳細分析體內的病毒耐受機制存在局限性。目前的COVID-19大流行使得解決這個謎團變得更加緊迫。
然而蝙蝠是野生動物,而不是馴養的實驗動物科目。對蝙蝠進行可重復的研究比對更常見的實驗動物如小鼠或豬進行更困難。因此,大多數實驗都必須在取自蝙蝠的細胞系上進行,而不是在蝙蝠本身或蝙蝠器官上進行。
“如果這一實驗性障礙能夠被克服,就可以理解病毒與蝙蝠的關系,從而減少人類疾病和死亡。”該論文的作者之一、東京農業技術大學傳染病流行病學和預防研究中心副教授Tsutomu Omatsu說。
因此,研究人員開發了可用于此類實驗的蝙蝠類器官。類器官是一種在“體外”(在培養皿或其他實驗室設備中)由干細胞培育而成的三維組織結構,它模仿了活體動物的器官。已知腸道是病原體與肺部一起進入和離開身體的通道之一。在這種情況下,他們從一種果蝠——棕果蝠(狐蝠科、果蝠屬動物,也被稱為果蝠)腸道細胞中培育出類器官。
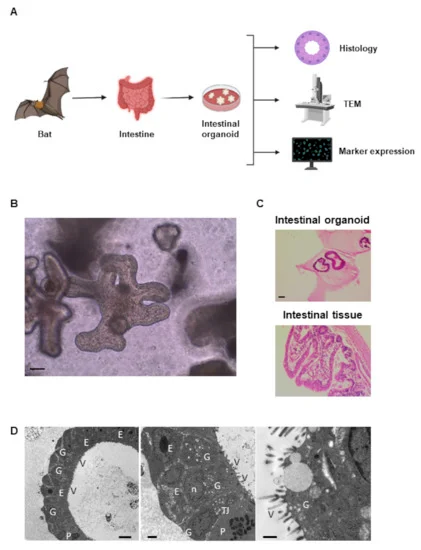
為什么選擇果蝠呢?果蝠是一種巨型蝙蝠,它們被認為是包括埃博拉病毒和馬爾堡病毒在內的病毒家族的天然宿主。之所以選擇棕果蝠,是因為在之前的研究中,已顯示出實驗性接種SARS-CoV-2(引起COVID-19的病毒)引起的短暫但不強烈的感染,而來自棕果蝠腸道的細胞系根本沒有被感染。東南亞和澳大利亞的幾種狐蝠也被發現是導致人類呼吸道疾病的PRV病毒的宿主。
研究人員首先必須找到一種最佳的蝙蝠腸細胞生長培養基。他們通過嘗試用九種不同的生長補充劑(營養素和其他促進細胞增殖的分子)培養類器官來做到這一點,包括Wnt 3a、Noggin、R-spondin (WNR)、EGF、FGF2、FGF7、FGF10、IGF或TGF-α。不同補充劑對果蝠類器官生長和增殖的影響存在顯著差異。七天后,其中三組(WNR、TGF-α、EGF)的細胞生長和增殖率顯著提高。然而,與對照組相比,FGF2、FGF7、FGF10和IGF沒有顯著影響。
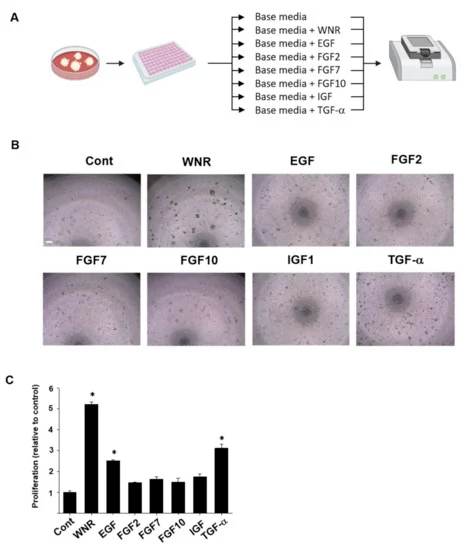
從果蝠中鑒定合適的腸類器官培養補充劑
基于這些結果,研究人員發現WNR、EGF和TGF-α對果蝠腸道類器官的培養至關重要。此外,用這三種補充劑生長的果蝠腸類器官壽命長,能夠保持活躍的增殖多達十代(從先前的類器官組成的分離細胞重建類器官的多達10倍)。長期冷凍保存(實質上是冷凍)的類器官一旦解凍也可以正常生長。
為了證實類器官是在模仿蝙蝠腸道的上皮(外部)組織——這是蝙蝠器官中最先遇到病毒顆粒的部分,因此具有特殊的科學意義,研究人員部署了兩種技術。首先,他們使用透射電子顯微鏡來研究類器官的細胞解剖學(組織學)。其次,他們使用免疫熒光染色,一種用于檢測和可視化生物樣品中分子的常用方法——來尋找分子標記物,表明所研究的組織來自蝙蝠的腸道。這兩種技術結合在一起告訴研究人員,類器官確實在重建果蝠腸組織的典型細胞成分。
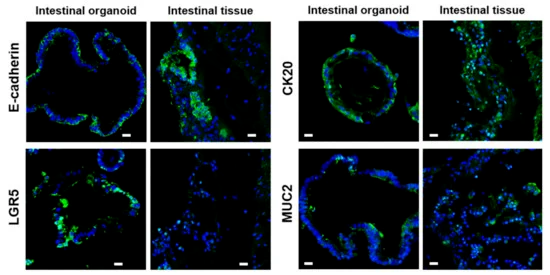
類器官再現了腸組織的細胞成分
還進行了使用類器官來研究病毒關系的初步測試。在實驗接種中,它們顯示對PRV敏感,但對SARS-CoV-2不敏感。
在首次成功制造出蝙蝠類器官后,研究人員現在想要在其他果蝠器官,如肺、肝和腎上重復他們的技巧。然后,研究人員將用高致病性病毒感染大量的蝙蝠“體內”,詳細分析它們的基因表達(打開和關閉基因),從而能夠闡明為什么蝙蝠能夠在不生病的情況下宿主這些病原體的機制。
參考資料:
https://medicalxpress.com/news/2021-12-intestine-organoid-grown-lab-viruses.html
| 我也說兩句 |
| 版權聲明: 1.依據《服務條款》,本網頁發布的原創作品,版權歸發布者(即注冊用戶)所有;本網頁發布的轉載作品,由發布者按照互聯網精神進行分享,遵守相關法律法規,無商業獲利行為,無版權糾紛。 2.本網頁是第三方信息存儲空間,阿酷公司是網絡服務提供者,服務對象為注冊用戶。該項服務免費,阿酷公司不向注冊用戶收取任何費用。 名稱:阿酷(北京)科技發展有限公司 聯系人:李女士,QQ468780427 網絡地址:www.arkoo.com 3.本網頁參與各方的所有行為,完全遵守《信息網絡傳播權保護條例》。如有侵權行為,請權利人通知阿酷公司,阿酷公司將根據本條例第二十二條規定刪除侵權作品。 |
 m.quanpro.cn
m.quanpro.cn